عندما نتأمل الجدول الدوري نجد أنه تزداد حجوم ذرات عناصر المجموعة الواحدة كلما اتجهنا إلى أسفل المجموعة في الجدول الدوري، حتى يتضح لنا تفسير ذلك نستعرض معكم عبر المقال أهم المعلومات عن الجدول الدوري، فقد أصبح من الأسئلة الشائكة لدى الطلاب في دراسة مادة العلوم وما صحة عبارة تزداد حجوم ذرات عناصر المجموعة الواحدة كلما اتجهنا إلى أسفل المجموعة في الجدول الدوري وما هو تفسيرها.
محتويات الصفحة
تزداد حجوم ذرات عناصر المجموعة الواحدة كلما اتجهنا إلى أسفل المجموعة في الجدول الدوري
هي بالطبع عبارة صحيحة ويفسر ذلك بأنه عندما نتجه إلى أسفل المجموعة في الجدول الدوري نلاحظ أن مستوى جديد أعلى من حيث الطاقة التي تكون حول النواة وبالتالي يزداد الحجم، مما يظهر لنا أن أحجام ذرات عناصر المجموعة الواحدة ازدادت وفقًا لزيادة طاقتها وهو بالطبع ما يعنيه أنه تزداد حجوم ذرات عناصر المجموعة الواحدة كلما اتجهنا إلى أسفل المجموعة في الجدول الدوري، كما يتم ترتيب العناصر في الجدول الدوري على مجموعات كل العناصر التي تتصف بسلوك كيميائي ذاته تكون في عمود خاص بها، وتكون الفلزات في جهة اليسار من الجدول، بينما تكون اللافلزات في جهة اليمين من الجدول الدوري.
تعرف أيضا : الجزيء الذي لا تتشارك فيه الالكترونات بصورة متساوية ..
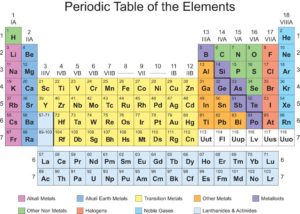
الجدول الدوري
هو عبارة عن جدول يضم ترتيب كل العناصر الكيميائية بحسب العدد الذري لكل منها ، ووفقُا للتوزيع الإلكتروني لها ، والسمات والصفات الكيميائية التي يتميز بها كل عنصر من العناصر الكيميائية عن غيره.
أهمية الجدول الدوري
يعد الجدول الدوري من الأدوات الهامة للغاية في مجال الكيمياء والعلوم التطبيقية، حيث يساعد مستخدميه في التعرف على العناصر الكيميائية وترتيبها وتتمثل أهمية الجدول الدوري فيما يلي
- تصنيف العناصر : يحتوي الجدول الدوري على العناصر الكيميائية كلها مما يتيح التعرف على العناصر الكيميائية التي تتميز بخصائص واحدة وصفات كيميائية ، حيث يتكون الجدول من مجموعات أفقية ورأسية ولكل عمود منها مجموعة تمتاز بنفس الصفات الكيميائية.
- التجارب القائمة على خصائص العناصر : يتم ترتيب العناصر الكيميائية في الجدول الدوري على حسب خصائصها وحجم طاقتها فمثلا نجد الفلزات في الجهة اليسرى من الجدول بينما اللافلزات في الجهة اليمنى مما يساعد في معرفة العناصر وخصائصها بسهولة عند إجراء التجارب العلمية.
تعرف أيضا : العامل المؤثر في عملية التحليل الكهربائي للماء ..
أعمدة الجدول الدوري
يحتوي الجدول الدوري على ثمانية عشر مجموعة مكونة من أعمدة طولية تم ترتيب العناصر بها بحيث تكون كل مجموعة منها لها نفس الخصائص الكيميائية كما تصنف المجموعات حسب خصائصها الطبيعية وعدد الإلكترونات الموجودة في المدارات الخارجية لكل عنصر.
كما تسمى الأعمدة الأفقية بالدورات ويتم تصنيفها حسب أعدادها الذرية، تنتهي كل دورة منها بعنصر خامل أو نبيل.
تحتوي المجموعة الثامنة عشر وهي من الأعمدة الطولية او الرأسية على عناصر خاملة أو نبيلة.
كما أن العناصر الموجودة في الثلاث مجموعات الأولى هي التي تفقد الكترونات، بينما باقي المجموعات تحتوي على العناصر التي تكتسب الكترونات، كما يضم الجدول الدوري في الأسفل سلسلة اللانثينيدا، وسلسلة الاكتينيدات.
بهذا قدمنا لكم عبر المقال لما تزداد حجوم ذرات عناصر المجموعة الواحدة كلما اتجهنا إلى أسفل المجموعة في الجدول الدوري، وما التفسير لذلك، وأهمية الجدول الدوري وتصنيف العناصر به.
[irp]







Leave a Comment